周福祥医生的科普号
- 精选 超低位直肠癌新辅助放化疗保肛-医学是艺术周福祥 主任医师 武汉大学中南医院 肿瘤放化疗科1731人已读
- 精选 低位直肠癌保肛策略---近距离放疗加量新辅助放化疗保肛
低位直肠癌手术治疗需要切除肛门,在腹部人造肛门,对患者生活质量带来一定影响,同时造口袋也有一定经济负担。直肠癌目前的标准治疗推荐是术前新辅助放化疗,可以降低复发率、提高治愈率。有多项研究表明术前新辅助放化疗联合局部加量放疗在低位直肠癌综合治疗中的价值,不仅可提高手术根治性切除率和保肛率,甚至高达40%的患者可在这种术前治疗策略结束后获得病理学完全性缓解(即显微镜下也没有癌细胞残存),从而降低术后复发率,提高远期生存率和长期生活质量。下面是我们的一个病例分享。患者何XX是湖北省广水市老师,2017年6月初无明显诱因出现血便,误以为是痔疮,当地治疗后无明显好转,后经人介绍于2017年6月21日至武汉大学中南医院结直肠肛门外科就诊,入院专科体检提示距肛缘3cm可及肿块下缘,肿瘤最大径约为3cm,肿块呈溃疡性变,肿块固定,界限相对明确,质脆,无明显触痛,双合诊提示肿块与阴道后壁下三分之一固定,指套退出少许染血。查血提示癌胚抗原CEA:124.9ng/mL↑。盆腔MRI提示直肠下段肿块,考虑直肠癌(图1);直肠中段右侧旁肿大淋巴结,考虑淋巴结转移(图2)。电子结直肠镜示齿线上缘可见一肿块,表面溃疡糜烂出血,占肠腔2/3(图3),并行直肠肿物活检术,术后病检示:腺癌。全身检查无明显转移。图1:直肠原发灶(红色箭头所指) A图为T1加权磁共振成像,提示直肠下段管壁明显增厚,内壁凹凸不平,管腔缩小,长度约3.5cm;B图为T1加权磁共振增强,提示直肠下段病灶呈明显欠均匀强化;C、D图为磁共振扩散加权成像,提示直肠下段病灶DWI呈稍高信号,相应ADC值降低。图2:淋巴结转移灶(红色箭头所指) A图为T1加权磁共振成像,提示直肠中段右侧旁见大小约13.6*12.6mm的等T1信号灶;B图为T1加权磁共振增强,提示直肠中段右侧旁结节呈明显环形强化;C、D图为磁共振扩散加权成像,提示直肠中段右侧旁结节DWI呈等信号,相应ADC值降低。图3:电子结直肠镜示齿线上缘可见一肿块,表面溃疡糜烂出血,占肠腔2/3。经上述系统分期检查,明确该患者诊断为直肠恶性肿瘤(腺癌),分期为cT3-4N+M0,Ⅲ期。请肿瘤中心放化疗胃肠肿瘤病区会诊后,建议患者先行新辅助放化疗,结合近距离放疗加量策略,争取最大降期或肿瘤完全消退。于2017年6月23日转入放化疗科进一步诊治。转入后,分别于6月30日、7月5日、7月24日行3次后装治疗(12Gy/3F),并于7月11日开始行直肠外照射调强放疗(IMRT),剂量为45Gy/25F,放疗期间给与亚叶酸钙+氟尿嘧啶同步化疗,放疗及化疗期间复查肿瘤标志物呈进行性下降,已降至正常(图4)。治疗后3周再次入院,复查提示直肠下段病变较前减轻(图5),直肠中段右侧旁淋巴结未见(图6)。电子结直肠镜示近肛缘见瘢痕,表面不规则溃疡,质地稍硬,取3块活检;超声内镜:粘膜层稍低回声病灶,局部粘膜下层欠清晰,固有肌层尚清晰直肠管壁外显示欠清晰。病检回报示:送检粘膜组织呈慢性活动性炎伴溃疡形成及淋巴组织增生。免疫组化检测,淋巴组织呈:CK(-),Ki-67(阳性率约为40%),P53(-),SMA(-)。图4:患者肿瘤标志物(CEA、CA724)检测结果图5:患者治疗后3周复查盆腔MRI提示直肠下段病变较前减轻。图6:患者治疗后3周复查盆腔MRI提示直肠中段右侧旁淋巴结消失。图7:患者治疗后3周复查电子结直肠镜及超声内镜结果。患者为直肠癌(cT3-4N+M0,III期),行术前新辅助放疗及化疗后,病灶达到病理完全缓解(pCR),继续新辅助化疗3周期后,于放疗后10周转至结直肠肛门外科行合适的外科治疗,在局部切除和根治性全系膜切除两种手术方案方面,患者选择根治性手术(全系膜切除即TME手术)并尽可能保留肛门功能,外科团队根据患者治疗意愿和肿瘤消退情况情况实施括约肌间切除的TME手术,保留了肛门功能,术后病理报告没有发现残存癌细胞(原发灶和淋巴结均阴性),病理学完全缓解。2018.10月复查没有复发转移,肛门功能满意。此病例很好得展示了术前新辅助放化疗联合近距离加量放疗在低位直肠癌综合治疗中的意义,术前新辅助放化疗不仅可提高手术根治性切除率和保肛率,甚至可达到完全性病理缓解率,降低术后复发率,提高远期生存率和长期生活质量。武汉大学中南医院肿瘤放化疗科是中南地区享有盛誉、历史最为悠久的肿瘤专科,是集医疗、教学、科研为一体的领航学科,是国家临床重点建设专科和肿瘤学国家疑难病诊治中心,是“十五”、“十一五”、“十二五”、“211”工程和“985”工程重点建设学科和湖北省重点学科。胃肠肿瘤亚专科率先开展院内多学科讨论模式,在胃癌、结直肠癌、胰腺癌、肝癌等消化系统恶性肿瘤的围手术期放化疗以及治疗的规范化、个体化治疗方面有着丰富的临床经验, 随着螺旋断层放疗(TOMO)和直肠腔内治疗的引入,将肿瘤的精准放疗提升到新的高度,造福于广大肿瘤患者。
周福祥 主任医师 武汉大学中南医院 肿瘤放化疗科3991人已读 - 精选 胰腺癌患者接受诱导化疗联合立体定向放疗的临床获益
一、病史概述1.患者某男,62岁2.主诉:腹膜后低分化腺癌术后2月余2015.10无明显诱因出现左上腹间断隐痛,于2016.1.25就诊于华中科技大学附属协和医院,行B超及CT示:肝胃韧带占位性病变。2016.2.15行腹膜后穿刺活检:低分化癌,免疫组化:PCK(+),CK7(灶状+),CK20(-), Villlin(+),Syn、S-100、LCA、CD117、P40(-),Ki67(LI:约90%),结合免疫组合,符合消化系统肿瘤浸润或转移。2016.2.22肠镜检查未见明显异常。2016.2.22行PET-CT:肝胃韧带、腹膜后区巨大软组织团块病变,与肝脏、胃贲门区及胰腺关系密切;网膜、系膜及腹膜后区多发淋巴结。患者于2016.3.4在协和医院胃肠外科行上腹部肿瘤切除+胰腺体尾部及脾脏切除+近端胃切除+食管远端胃吻合,术中见左肝脏面下方与胃小弯侧及胃后网膜囊和胰腺体部前上方及肠系膜上动脉以上腹主动脉前方见一直径约13cm*11cm实质性肿瘤,与胰腺体部及近端胰尾融合为一体,与小弯邻近贲门及近端胃体侵犯融合,肿瘤将腹腔干及分支完全包裹。术后病检:(胰体尾、脾脏、肝胃间隙)低分化癌浸润胰腺,侵犯胃壁(由浆膜外浸润至固有肌层),侵犯小网膜;脾脏、贲门断端及胃体断端、胰腺切缘、胰尾、大网膜切片上未见癌累及。小弯侧淋巴结(19枚)、周围系膜淋巴结(5枚)未见癌转移。免疫组化:PCK(+),CK7(灶状+),CK20(-),Villlin(+), CDX2(-), HER2(0),Syn(-),CgA(-),CK5/6(小灶+),P40(个别+),P63(个别+),CD56(-), PAS染色(少量细胞+),粘液染色(局灶间质+)。考虑低分化腺癌。KRAS、NRAS、BRAF、PIK3CA未见突变。3.既往史:2007年脑溢血病史,否认其他特殊病史。4.体检:KPS=100分,浅表淋巴结未及肿大,腹部可见陈旧性手术疤痕,心肺腹体检未见明显异常。5.辅助检查:2016.5.12,术后2个月胸部CT:左侧胸腔少量积液;左下肺纤维灶.骨ECT:未见明显异常.腹部MRI:腹腔、腹膜后多发结节及肿块,包绕腹腔大动脉.入院诊断:胰腺低分化腺癌术后(pT4N1M0,R2)复发图1:腹部MRI:腹腔、腹膜后多发结节及肿块,包绕腹腔大动脉(2016.5.12,术后2个月)二、诊疗经过腹膜后肿块MRI图像变化如下图所示:三、体会与思考本文分享了一例胰腺低分化腺癌患者通过诱导化疗后联合立体定向放射治疗(Stereotactic body radiation therapy ,SBRT),有效缓解症状及改善预后的病例。80%的胰腺癌患者在确诊时已至中晚期,预后极差,5年生存率仅为8%, 中位生存时间9~11个月[1]。根据中华医学会外科学分会胰腺外科学组发布的《胰腺癌诊治指南(2014)》,对于不可切除的局部进展期或转移性胰腺癌,积极的化学治疗有助于缓解症状、延长生存期及改善生活质量。根据病人体能状态,可选择的方案包括:吉西他滨单药( Category 1),吉西他滨﹢氟尿嘧啶类药物( Category 1),吉西他滨+白蛋白结合型紫杉醇( Category 1), FOLFIRINOX 方案( Category 1)等[2]。对于全身状况良好的不可切除的局部晚期胰腺癌,采用以吉西他滨或氟尿嘧啶类药物为基础的同步放化疗或诱导化疗后放疗可有效缓解症状及改善病人预后。同步放化疗中放疗剂量为50~54Gy,每次分割剂量为 1.8~2.0Gy[3]。尽管上述为期5~6周的标准放化疗方案可以改善局晚期胰腺癌患者的局部控制率,但是常规分割剂量延长了全剂量全身治疗的时间,而且常规放射治疗患者有60%以上因不良反应大而中断治疗[4]。SBRT能使靶区获得高剂量照射,靶区外正常组织受照射剂量减少,治疗时间短,从而达到提高局部控制率,减少肿块复发的治疗效果[5]。点评:胰腺癌对常规分割放射治疗响应性低,局部控制差。近年来,随着放射治疗设备和临床应用经验积累,国内外治疗应用SBRT胰腺癌的探索逐步增多。上腹部肿瘤SBRT关键在于对周围危及器官(OARs)的保护,除了传统需要保护的OARs如肝肾之外,周围空腔器官如胃、十二指肠、空肠对大剂量分次放疗十分敏感,剂量限制把握不好极易导致急性和晚期放射损伤。临床实践中,医生和物理师要充分利用SBRT靶区剂量非均匀性的特点,合理运用放射生物学模型,设定OARs的限定参数,保证正常组织并发症发生率在可接受的范围内,避免盲目开展上腹部肿瘤SBRT的潜在风险。参考文献:[1] Siegel RL, Miller KD, Jemal A: Cancer statistics, 2016. CA Cancer J Clin. 2016;66 (1):7-30.[2] Ware MJ, Curtis LT, Wu M, Ho JC, Corr SJ, Curley SA, Godin B, Frieboes HB. Pancreatic adenocarcinoma response to chemotherapy enhanced with non-invasive radio frequency evaluated via an integrated experimental/computational approach. Sci Rep. 2017;7(1):3437. [3] Chang JS, Chiu YF, Yu JC, Chen LT, Ch'ang HJ: The Role of Consolidation Chemo-Radiotherapy in Locally Advanced Pancreatic Cancer Receiving Chemotherapy: An Updated Systematic Review and Meta-Analysis. Cancer Res Treat. 2017 Jun 9. doi: 10.4143/crt.2017.105. [Epub ahead of print][4] Krishnan S, Chadha AS, Suh Y et al. Focal Radiation Therapy Dose Escalation Improves Overall Survival in Locally Advanced Pancreatic Cancer Patients Receiving Induction Chemotherapy and Consolidative Chemoradiation. Int J Radiat Oncol Biol Phys. 2016;94(4):755-765.[5] Rosati LM, Kumar R, Herman JM. Integration of Stereotactic Body Radiation Therapy into the Multidisciplinary Management of Pancreatic Cancer. Semin Radiat Oncol. 2017;27(3):256-267.
周福祥 主任医师 武汉大学中南医院 肿瘤放化疗科2068人已读 - 精选 消化系统肿瘤疾病常识
一、胃癌 流行病学:胃癌是全世界的重要健康问题,东亚地区尤其高发,也是我国常见的恶性肿瘤之一,中国西北与东部沿海高于南方地区,在我国其发病率居各类肿瘤的首位。在胃的恶性肿瘤中,腺癌占95%。 危险因素:外源性因素主要是幽门螺旋杆菌感染、胃反流、慢性萎缩性胃炎、残胃;长期食用熏烤、腌制食品;食物中缺乏新鲜蔬菜、水果;吸烟高于不吸烟50%等。内源性因素则与家族史密切相关。 临床表现:1)早期无明显症状或仅有上腹部不适、不典型的上腹部疼痛、食欲减退、饱胀、嗳气。少数可有黑便或呕血。2)中晚期胃癌呈进行性消瘦、贫血、低蛋白血症、浮肿、恶病质;可出现持续性上腹痛;可有呕血及黑便。 治疗方案:最好在还未进行任何治疗之前,就采取多学科治疗方案,包括:肿瘤外科、肿瘤内科、消化内科、放疗科和病理科等。 二、结直肠癌 流行病学:是常见的消化道恶性肿瘤,占胃肠道肿瘤的第二位。好发部位为直肠及直肠与乙状结肠交界处,占60%。发病多在40岁后,男女之比为2:1。 危险因素:研究指出,生活方式、精神刺激、烹调方式不当、饮食油腻等、肠道相关症状或疾病、家族肿瘤史与结直肠癌的发生有关;而轻体力活动、饮茶、奶制品、膳食纤维为保护性因素,为结直肠癌的早期预防提供了科学依据。 临床表现:早期多无症状,病人无明显体征;中晚期临床特征主要为便血和排便习惯改变。 治疗原则:大肠癌的治疗以手术切除癌肿为首选,辅之以放射治疗、化疗药物治疗等;最近不少学者对早期大肠癌采用经内镜下切除治疗,也取得较好疗效。至于如何选择最佳方案,须依据不同的临床病理分期。 三、肝癌 流行病学:原发性肝细胞癌(HCC,简称肝癌)是常见恶性肿瘤之一。全球以东南亚与非洲撒哈拉沙漠以南(新加坡、泰国、菲律宾、中国、日本、莫桑比克、南非、马来西亚、印尼等)高发。英、美、北欧等发病率较低。 危险因素:病毒性肝炎(乙型、丙型、丁型)-我国肝癌90%有乙肝背景;另外与黄曲酶毒素、饮水污染、吸烟、饮酒、遗传因素等有关。 临床表现:早期多无症状;晚期多以腹痛为首发症状,纳差、消瘦、腹胀、发热、黄疸及其它:出血倾向—牙龈出血,鼻纽; 腹泻、右肩痛(易忽略)等。 治疗方案:以手术为主的综合治疗;局部肿块较大者,可结合射频、栓塞或放射治疗。 日期
周福祥 主任医师 武汉大学中南医院 肿瘤放化疗科3120人已读 - 精选 低位直肠癌,疾病不幸,医患有情,保留肛门,治好癌症
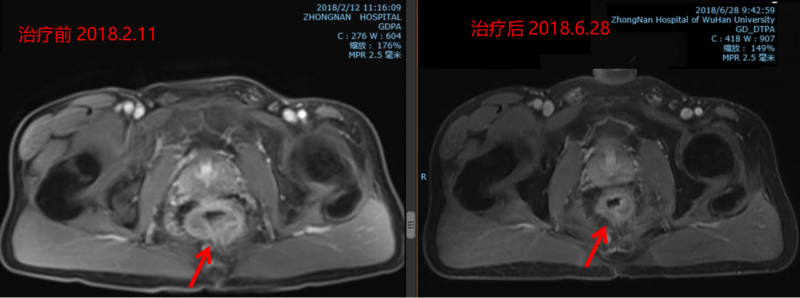
基本信息Z,男,46岁,大便性状改变及便血半年。既往史及家族史无特殊;ECOG评分:0分血生化:血常规、肝肾功能未见明显异常,肿瘤标记物:2018.2.12 CA199229.50U/mL↑。检查:心肺腹无明显异常。直肠指诊:肛门括约肌张力正常,距肛门约2.5cm处触及一明显肿块,肿块环肠壁一周,上达指尖,退指指套染血。电子肠镜(2018.2.12):距肛门4-9厘米见环形新生物,表面溃烂,质脆。探头置直肠病变处见环周低回声病灶,部分病灶突破外膜层,壁外见低回声淋巴结,部分病变与前列腺分界欠清晰。病理结果:(直肠活检)腺癌。腹盆腔MRI(平扫+增强)(2018.2.11):直肠下段(距肛缘3.8cm)管壁增厚直肠系膜多发小淋巴结,直肠左旁软组织肿块,考虑肿大淋巴结;肝多发囊肿。考虑直肠癌(T3N2Mx)双肺数枚微结节,多考虑炎性增殖灶,建议定期复查。诊断:直肠恶性肿瘤(腺癌)cT3N2M0,Ⅲ期。治疗经过:保肛意愿强烈,确诊时正值除夕,当天开始化疗FOLFOX6一周期,春节后开始腔内后装放疗3次,肿块明显缩小,便血未再出现。随后开始盆腔TOMO放疗+3FOLFOX6同步化疗。CA199逐步降至正常。三个月后复查腹盆腔MRI直肠病灶和淋巴结明显缩小,电子肠镜:(2018.6.28)(直肠活检)送检少许直肠粘膜组织呈轻度慢性活动性炎,另见少量变性坏死及炎性渗出组织。补充化2FOLFOX6。2018.07.04保留肛门根治手术,术后原发灶仅少许腺癌细胞。术后大便次数增多,药物对症治疗后逐步好转,工作生活恢复正常。4年后复查未见肿瘤,肛门控制良好。
 周福祥 主任医师 武汉大学中南医院 肿瘤放化疗科259人已读
周福祥 主任医师 武汉大学中南医院 肿瘤放化疗科259人已读





